Nous avons collaboré avec Eli Lilly pour présenter nos recherches sur les réactifs recombinants et la technologie microfluidique pour les tests d’endotoxines bactériennes (TEB) lors de la conférence sur la microbiologie pharmaceutique de la Parenteral Drug Association (PDA).
Nos résultats, basés sur des données d’échantillons réels, démontrent la précision et la fiabilité des agents recombinants sur les plateformes de détection microbiologique modernes. Jay Bolden et Hayden Skalski présentent leurs recherches à la PDA Microbiology Conference.

Contexte : Lysat d’amibocytes de limule (LAL) vs. réactifs en cascade recombinants (rCR) dans les tests TEB microfluidiques
Les entreprises pharmaceutiques adoptent de plus en plus des technologies innovantes afin de répondre aux attentes réglementaires en constante évolution tout en mettant en place des opérations plus durables. Les tests d’endotoxines sont un excellent exemple de ce changement, car les pressions réglementaires et de durabilité transforment le paysage des TEB. L'annexe 1 encourage les progrès technologiques visant à rationaliser les processus de production, et la récente publication de l'USP <86> sur les réactifs recombinants pour les tests d'endotoxines représente une opportunité clé pour respecter à la fois les normes en vigueur et les objectifs de durabilité.
Pour ces raisons, Veolia, en partenariat avec Eli Lilly, a mené une étude comparative à l’aide de la plateforme de test d’endotoxines bactériennes (TEB) Eclipse de Sievers afin de comparer les résultats entre le lysat d’amibocytes de limule (LAL) traditionnel et les réactifs en cascade recombinants (rCR) plus récents. La plateforme utilise la microfluidique et la force centripète ; elle permet de configurer les tests en 85 % du temps nécessaire à la configuration d'une microplaque traditionnelle à 96 puits ; elle utilise jusqu'à 90 % moins de LAL ou de rCR ; et elle automatise l'administration du LAL aux échantillons. Au-delà de l’augmentation de l’efficacité, il garantit des résultats précis et exacts, permettant aux fabricants d’atteindre l’annexe 1 et les objectifs de durabilité tout en restant en totale conformité avec les réglementations pour assurer la sécurité des patients.
Cette recherche présente les résultats des tests d’endotoxines avec des données obtenues à partir d’échantillons réels, fournissant une comparaison pratique entre les deux types de réactifs.
Étude comparative : Détection des endotoxines naturelles (NOE) et de l’endotoxine étalon de référence (RSE)
L’objectif de cette étude était motivé par deux objectifs. L’objectif principal était d’évaluer la détection et la récupération des endotoxines naturelles (NOE) et de l’eau purifiée dopée avec de l’endotoxine standard de référence (RSE). Cette évaluation a été réalisée à l’aide de deux méthodes de test différentes : le lysat d’amibocytes de limule traditionnel (LAL) et le réactif en cascade recombinant (rCR), dans le but de démontrer une récupération fiable des endotoxines sur les deux plateformes de test.
Deuxièmement, ces capacités ont été validées sur la plateforme Eclipse TEB de Sievers en la testant avec les deux types de réactifs. Cette validation était particulièrement importante car elle visait à démontrer l’adéquation du système aux tests sur échantillons en conditions réelles tout en offrant deux avantages substantiels : une réduction de 90 % de la consommation de réactifs et la possibilité d’utiliser des réactifs recombinants, promouvant ainsi des pratiques de test plus durables dans l’industrie.
Echantillons : étude comparative rCR de 12 types d’échantillons
Les échantillons suivants ont été utilisés dans l’étude comparative entre le lysat d’amibocytes de limule (LAL) et les réactifs en cascade recombinants (rCR) :
- Deux anticorps monoclonaux
- Insuline
- Peptide
- NOE (voir Figure 1)
- Histidine et acétate de sodium
- LRW
- Eaux purifiées
- Eaux purifiées avec pics RSE
- Polysorbate 80
- Produits contrefaits
- Composants (bouchon, cartouche)
- Yeastolate
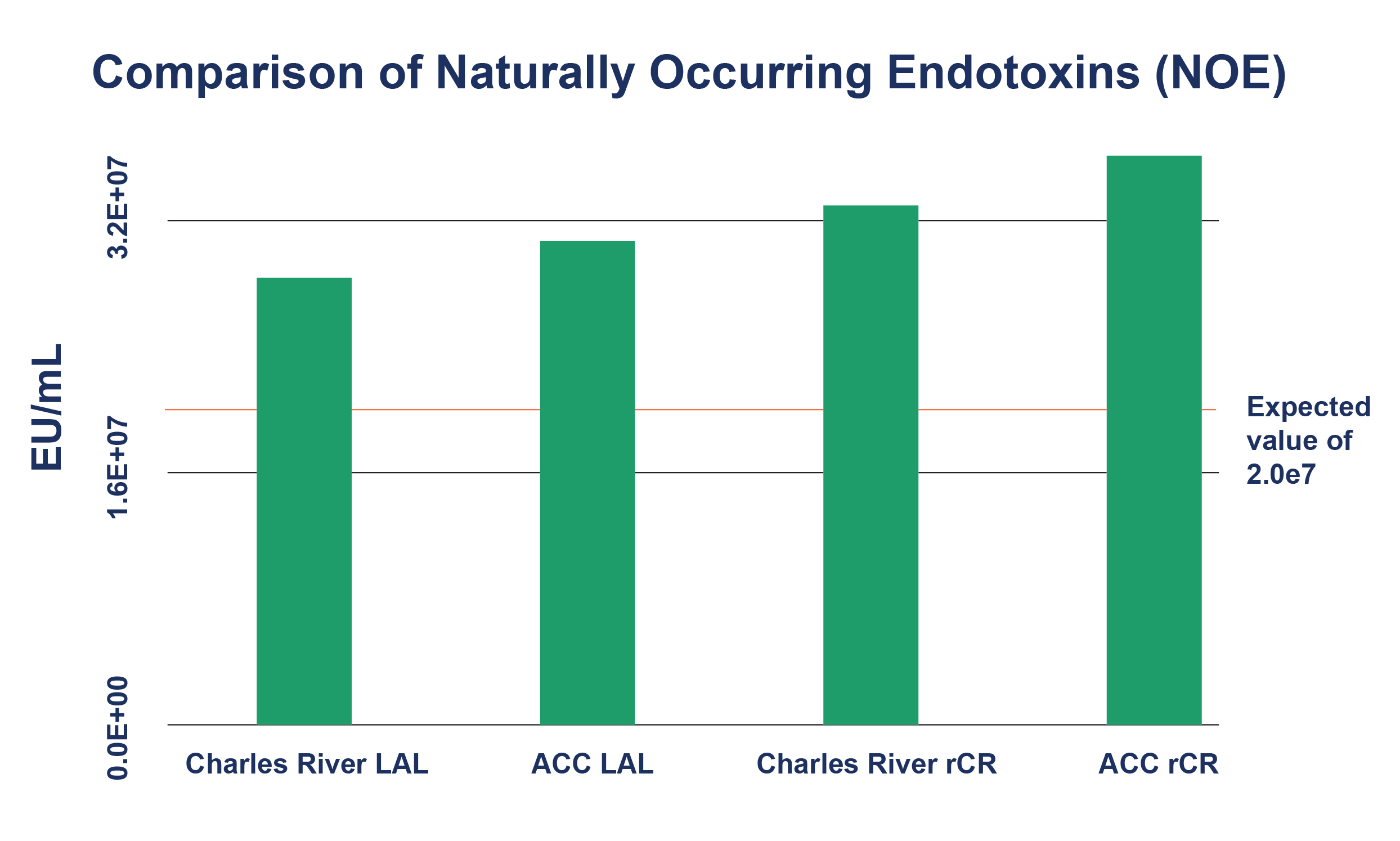
Figure 1 : comparaison des endotoxines naturelles (NOE)
Résultats : LAL vs rCR - résultats des performances et des tests
La figure suivante détaille les taux de récupération par contrôle positif des produits (PPC) de l’échantillon et des réactifs.
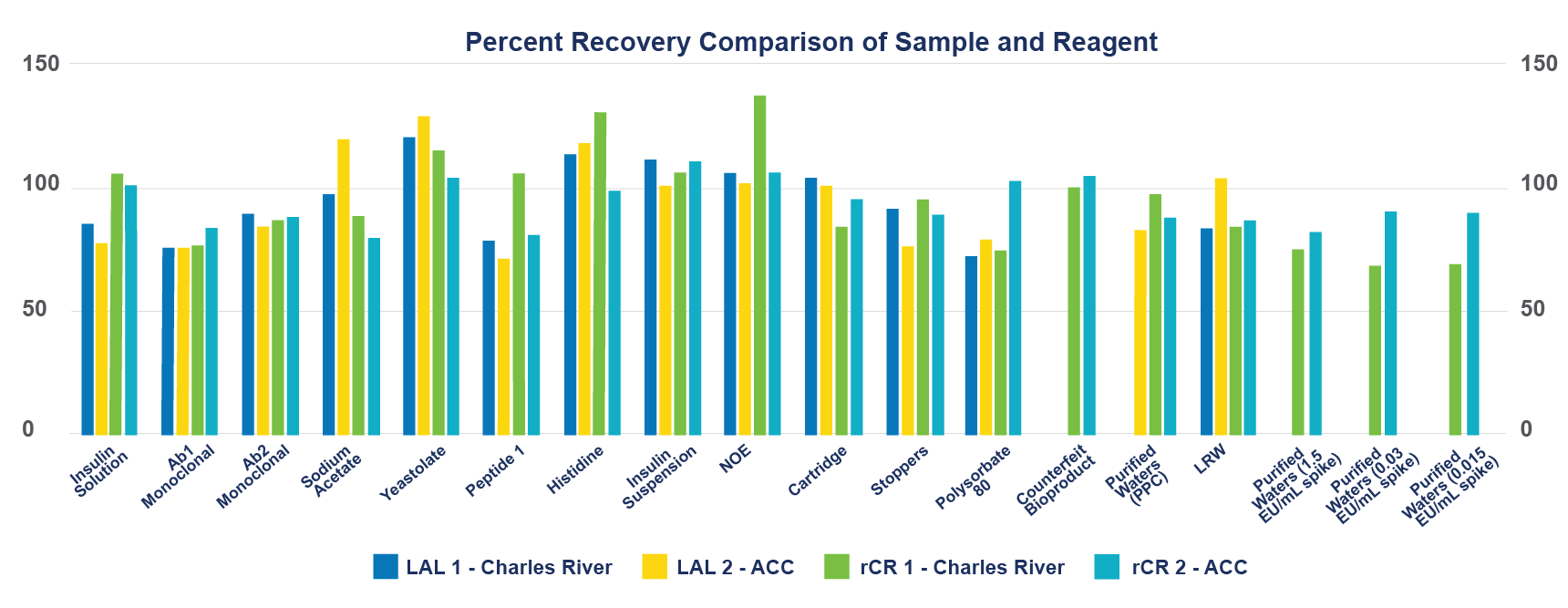
Conclusion : performance de la rCR dans les plateformes microfluidiques
Cette étude a montré des performances équivalentes entre le LAL et le rCR en utilisant le Sievers Eclipse pour détecter les endotoxines bactériennes dans des échantillons réels, ainsi que des endotoxines naturelles. Sur la base des éléments disponibles, il est possible de conclure que la plateforme de test des endotoxines bactériennes Sievers Eclipse est capable d'utiliser avec succès les réactifs en cascade recombinants, à condition que la compatibilité de l'échantillon ait été vérifiée.
L’automatisation via la plateforme microfluidique centripète de l’Eclipse offre la forme la plus simple de microfluidique TEB disponible, offrant un gain de temps significatif et réduisant les risques d’erreur. Grâce à la disponibilité de cette technologie innovante, les tests TEB peuvent être rationalisés tout en restant entièrement conformes à la pharmacopée.
Les avantages incluent :
- Conforme aux normes USP <85> et <86>
- Efficacité éprouvée avec les réactifs LAL et rCR
- Jusqu’à 90 % de réactif en moins nécessaire ; contribue aux initiatives en matière de durabilité
- 27 étapes de pipetage au total pour 21 échantillons pour une efficacité accrue
- Technologie innovante conforme aux lignes directrices de l’annexe 1
En savoir plus sur le Sievers Eclipse
Auteurs :
- Jay Bolden
-
Jay Bolden est directeur principal au sein de l’organisation mondiale de contrôle de la qualité analytique d’Eli Lilly and Company. Il est un expert en endotoxines bactériennes et dirige une équipe chargée de superviser le contrôle qualité mondial des méthodes de test des endotoxines, de la microbiologie et de la virologie. Jay est titulaire d’une licence en biologie et d’un certificat en études environnementales de l’Université de l’Indiana et possède plus de 25 ans d’expérience dans l’industrie dans les domaines du développement, de la microbiologie des procédés et des laboratoires, ainsi que de la direction de laboratoires de microbiologie. Jay est membre du comité d’experts en microbiologie de la pharmacopée des États-Unis et est l’auteur d’un chapitre de livre et de plusieurs articles évalués par des pairs sur les endotoxines. Contenu accordéon 1.
- Meg Provenzano
-
Meg Provenzano est cheffe de produit mondiale pour les instruments de bio-détection Sievers chez Veolia. Elle possède plus de 10 ans d'expérience dans le secteur des tests d'endotoxines bactériennes et a occupé plusieurs postes liés au contrôle de la qualité, à l'assistance technique et à la gestion des produits. Avant de rejoindre Veolia, Meg était chef de produit chez Charles River Laboratories. Elle est centrée sur le client et aime résoudre les problèmes de manière pratique, qu'il s'agisse de questions techniques, d'assistance pour les analyses ou de logiciels. Meg est titulaire d'une licence en sciences marines et biologie de l'université Coastal Carolina, où elle s'est spécialisée dans la recherche sur la population des grands dauphins.
- Brian Short
-
Brian Short est spécialiste mondial des applications pharmaceutiques chez Veolia, où il fournit un soutien stratégique en matière de biodétection pharmaceutique et d'applications COT pour l'industrie des sciences de la vie. Avec 20 ans d’expérience de travail dans et avec des laboratoires de contrôle de la qualité pharmaceutique, Brian a supervisé et soutenu de grands volumes d’essais en cours de fabrication et de produits finis. Ayant précédemment occupé des postes chez Wyeth et Lonza, et fort de neuf ans d’expérience dans le soutien de la gamme de produits Sievers au sein de GE Analytical Instruments, SUEZ et maintenant Veolia, Brian possède une expertise approfondie des instruments et des logiciels de détection des endotoxines, y compris l’installation, la qualification et la formation. Brian est titulaire d'une licence en sciences biologiques du York College of Pennsylvania.
- Hayden Skalski
-
Hayden Skalski est le spécialiste de l’application des produits pour les sciences de la vie chez Veolia, spécialisé dans les tests d’endotoxines bactériennes (TEB). Hayden a plus de 10 ans d’expérience dans l’industrie pharmaceutique et le contrôle de la qualité microbiologique et a fait des présentations sur de nombreux sujets entourant les tests d’endotoxines. Auparavant, Hayden a occupé des postes chez Charles River Laboratories, Regeneron et Novartis, où il a validé et exécuté des protocoles de développement de méthodes pour les tests d’endotoxines, en assurant l'assistance à la clientèle, le dépannage et la prise en charge des tests de produits en grand volume. Hayden est titulaire d’un B.S. de l’Université d’Albany (SUNY) en biologie. Kelly Smith est biologiste principal au sein de l’organisation mondiale de contrôle de la qualité analytique d’Eli Lilly and Company. Il est un expert en endotoxines bactériennes avec plus de 25 ans d’expérience dans l’industrie et est titulaire d’une licence en chimie de l’Université Butler.
- Kelly Smith
-
Kelly Smith est biologiste principal au sein de l’organisation mondiale de contrôle de la qualité analytique d’Eli Lilly and Company. Il est un expert en endotoxines bactériennes avec plus de 25 ans d’expérience dans l’industrie et est titulaire d’une licence en chimie de l’Université Butler.
